更新日:2020年7月25日
エタノールの沈殿の原理

エタノール沈殿(エタ沈)とは
エタノール沈殿(通称エタ沈)は、水溶液中の核酸(DNAまたはRNA)の濃縮あるいは脱塩によく使用される手法です。本記事では、エタノール沈殿法の原理を塩とエタノールの役割から説明します。
エタノール沈殿の操作概要
まず、水溶液に塩とエタノールを加え、溶液中の核酸を沈殿させます。次に、遠心分離により核酸ペレットを形成させます。核酸ペレットを70%エタノールで洗浄し、さらに遠心分離ステップを行った後、エタノールを除去します。最後に、核酸ペレットを乾燥させてから、バッファーに再懸濁します。
溶解性の制御がエタノール沈殿の原理
核酸が水に溶ける理由を説明します。
水は極性分子です。水分子は、酸素原子の近くに部分的な負電荷があり、水素原子の近くに部分的な正電荷があります(下図を参照)。
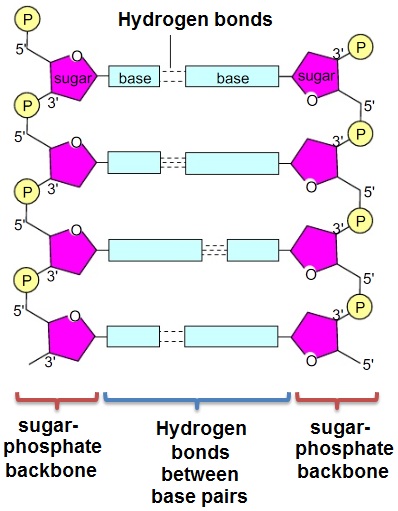
DNAとRNAは、負に帯電したりん酸(PO3-)基が主鎖にあるため極性分子です 。同じく極性分子である水分子と静電的相互作用し、水に容易に溶解します。したがって、核酸のような極性分子は親水性と言い換えられ、一方で水分子と容易に相互作用できない非極性分子は疎水性と言えます。
エタノール沈殿法を簡潔に言うと、 核酸のりん酸(PO3-)に由来する負の電荷を塩で中和し、水よりも極性の低いエタノールで核酸の親水性(水への溶解性)を低下させる操作です。
詳細を説明していきます。
エタノール沈殿における塩の役割
エタノール沈殿における塩の役割は、核酸の糖-りん酸骨格の負の電荷を中和することです。
エタノールは水よりも極性が低いため、核酸溶液にエタノールを加えることで、核酸の水への溶解性を低下させる作用があります。一見するとエタノールのみでエタノール沈殿法は成立しそうに思えます。
しかし、核酸はエタノールだけでは沈殿しません。その理由は、核酸がりん酸(PO3-)に由来する負の電荷を持つからです(下図のPの部分)。
核酸全体が負の電荷であるため、エタノールによって核酸の水溶性が低下したとしても、核酸分子が負の電荷同士で反発しあい、核酸の凝集が起こりにくいのです。
そこで、塩の力を借りて核酸の負の電荷を中和します。
一般的に使用される塩は酢酸ナトリウムです。溶液中で、酢酸ナトリウムはNa +と[CH3COO]-に分解します。正に帯電したナトリウムイオンは、核酸の りん酸(PO3-)基の負の電荷を中和します。これにより、負の電荷同士の反発がなくなり核酸は凝集しやくすくなります。
エタノール沈殿におけるエタノールの役割
上記でも述べましたが、エタノールは水よりも極性が低いため、核酸溶液にエタノールを加えることで、核酸の水への溶解性を低下させる作用があります。しかし、エタノールが必要な理由はそれだけではありません。
水の中では先程説明したNa + とりん酸(PO3-)の結合が起こりにくく、エタノールを加えることで Na+によるりん酸(PO3-) の負電荷の中和が成立するのです。
溶液中のNa +イオンとPO3-イオン間の静電力は、クーロンの法則によって決まります。クーロンの法則は、溶液の誘電率の影響を受けます。水は誘電率が高いため、Na +とPO3-が結合するのは困難です。一方、エタノールの誘電率は低いため、Na +がPO3-と相互作用し、電荷が中和されます。
エタノール沈殿原理のまとめ
- 塩の役割
核酸分子同士の結合反発を抑制するために、Na+でりん酸(PO3-)基に由来する核酸の負の電荷を中和する。これにより核酸が凝集しやくすくなります。 - エタノールの役割
水よりも極性が低いため、核酸の水溶性を低下させる。
Na+とりん酸(PO3-)基の結合を促進する。
エタノール沈殿のプロトコル:方法

用意する試薬
・100% エタノール
・70% エタノール(冷蔵庫で冷やしておく)
・3mol/l 酢酸ナトリウムバッファー, pH 5.2(冷蔵庫で冷やしておく)
・1xTEバッファー
3mol/l 酢酸ナトリウムバッファー, pH 5.2とTEバッファーの作り方はこちら
プロトコル
- サンプルの溶液量に対し、1/10量の3mol/l 酢酸ナトリウムバッファー, pH 5.2と2-3倍量の100% エタノールを添加し、ボルテックスミキサーで混合します。
- -20℃で一晩凍結します。もしくは、10-15分間ドライアイスで冷やします。
- 13,000rpmで30分間4℃で遠心分離します。チューブ底に核酸のペレットができます。
- 上清をデカンテーションまたはピペッティングで取り除きます。
Note:ペレットが見えない場合や浮いてしまった場合は、再度13,000rpmで30分間4℃で遠心分離します。 - ペレットを乾燥させます。チューブのフタを開いて15分間程度静置します。
Note:乾燥させすぎるとペレットが溶解しにくくなります。ペレットが湿っている状態で乾燥をやめます。 - TEバッファー(10mM Tris-HCl、pH7.5、1mM EDTA)か水を加え、ペレットを溶解させます。
こちらもチェック!
各社のエタノール(JIS:試薬特級)の価格比較|最安値は?
アガロースゲルの作り方と適切な濃度:電気泳動
植物からゲノムDNAを抽出する方法・プロトコル
参考文献
Ichiro Hirao et al.,第一回エタノール沈殿, 実験医学オンライン, 羊土社.
Nick Oswald, Ethanol Precipitation of DNA and RNA: How it works, BiteSizeBio.
Yours Truly, DNA and RNA (A2), A chemblog.
OpenWetWare, Ethanol precipitation of nucleic acids.










コメントを残す