植物からのDNA抽出について
植物からの適切なDNAの単離は植物研究において必須です。
植物からの適切なDNA抽出方法は、植物の種類、使用する植物の部位、生育環境、植物の生長段階によって異なり、一定レベルのDNAの量と質を維持するのは簡単ではありません。例えば、穀類は炭水化物が豊富なのに対し、薬用植物はポリフェノールが豊富で、ストレスを受けた植物はポリフェノールが多く含まれています。植物の葉のサンプルにはポリフェノール、タンニン、多糖類が多量に含まれています。サンプルに含まれるこれら分子はDNA抽出においては阻害要因となるため、サンプルによってDNA抽出方法を変えることは珍しくありません。
DNA抽出に使用する植物組織は、一般的に15-20日齢の新鮮なものが好ましく、通常はまず乳棒(Pellet pestle)や破砕機で物理的に構造を壊します。DNA の単離の基本原理は、細胞壁、細胞膜、核膜を破壊し、DNAを沈殿させてタンパク質、多糖類、脂質、フェノール類、その他の代謝物など不要な分子を酵素的または化学的方法で除去します。
植物DNAの抽出試薬は、ドデシル硫酸ナトリウム(SDS)ベースのバッファーかCTAB(Cetyl trimethyl ammonium bromide)ベースのバッファーがよく使用されます。ここでは、ドデシル硫酸ナトリウム(SDS)ベースのEdward extraction bufferを用いた植物DNAの抽出方法を紹介します。
植物DNAの抽出に必要な試薬

- 70%エタノール
- イソプロパノール
- Edward extraction buffer(作り方は後述)
- トリス(Edward extraction bufferの作製に使用)
- EDTA・2ナトリウム・2水和物(Edward extraction bufferの作製に使用)
- 塩化ナトリウム(Edward extraction bufferの作製に使用)
- ドデシル硫酸ナトリウム(Edward extraction bufferの作製に使用)
- 精製水(Edward extraction bufferの作製に使用)
Edward extraction bufferの組成と作り方(50mL)
以下の表の従い混合して作製します。
- 「1mol/L トリス溶液, pH8.0」と「0.5mol/L EDTA溶液, pH8.0」の作り方はこちらのページに記載しています。
- 「5mol/L 塩化ナトリウム溶液」は、塩化ナトリウム粉末29.22gへ100mLの精製水を加えて作製します。
- 「10w/v% ドデシル硫酸ナトリウム溶液」は、ドデシル硫酸ナトリウム10gを100mLの精製水に溶解して作製します。
| 試薬 | 使用量 |
| 1mol/L トリス溶液, pH8.0 | 10.0mL |
| 0.5mol/L EDTA溶液, pH8.0 | 2.5mL |
| 5mol/L 塩化ナトリウム溶液 | 2.5mL |
| 10w/v% ドデシル硫酸ナトリウム溶液 | 2.5mL |
| 精製水 | 32.5mL |
植物DNAの抽出に必要な装置・機器類
- Pellet pestle
- 遠心分離機
- ボルテックスミキサー
Pellet pestleはマイクロチューブ内で組織を破砕する道具です。
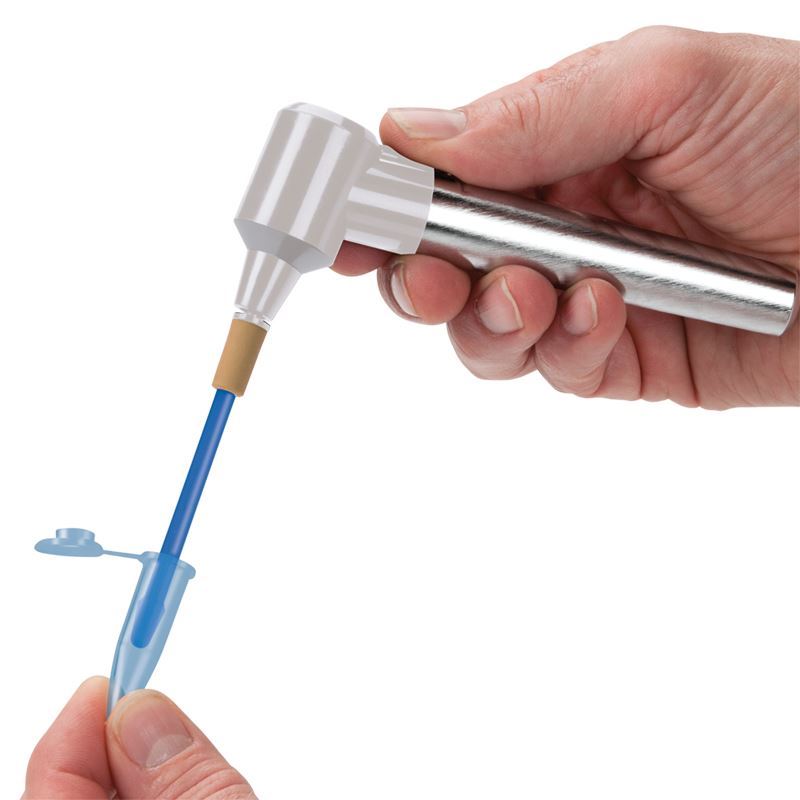 出典:PESTLE MOTOR FOR PELLET PESTLE MIXERS, CORDLESS
出典:PESTLE MOTOR FOR PELLET PESTLE MIXERS, CORDLESS植物のゲノムDNAの抽出方法:プロトコル

- マイクロチューブに植物の組織を入れ、Pellet pestleで組織をつぶします。
葉を使用する場合は1-2枚分をチューブに入れます。 - Edward extraction bufferを400μL取り、つぶした組織に添加します。
- ボルテックスミキサーで5秒間混合します。
- 遠心分離機を使い、16,000rpmで2分間室温で遠心します。
- 上清を300μL取り、別のマイクロチューブへ移します。
- イソプロパノール300μLを添加し、ボルテックスミキサーで混合します。
- 室温で2分間静置します。
- 遠心分離機を使い、16,000rpm室温で5分間遠心します。
- デカンテーションかピペットで上清を捨てます。
- 残ったペレットに70%エタノールを700μL添加します。
- 遠心分離機を使い、16,000rpm室温で5分間遠心します。
- 上清を捨てます。
なるべく多くの上清を捨てた方が次の乾燥を短時間にできますが、ペレットを捨ててしまわないように注意しましょう。 - マイクロチューブのフタを開け、エタノールが揮発してなくなるまで室温で静置します。
ペレットが乾燥しすぎると溶解しにくくなります。 - 40-100μLの精製水かTEバッファーをペレットへ添加し、ボルテックスミキサーで混合します。
以上で終了です。-20℃で保管します。
植物DNAの抽出操作がわかる動画
上記プロトコルとはやや異なりますが、操作方法がよくわかる動画です。
市販の植物DNA抽出キット

植物組織からDNAを抽出する市販キット例です。スピンカラム法と磁気ビーズ法のキットを紹介します。
スピンカラム法ISOSPIN Plant DNA
- ISOSPIN Plant DNA:ニッポンジーン
- DNeasy Plant Mini Kit:Qiagen
- PureLink™ Genomic Plant DNA Purification Kit:Thermo Fisher Scientifc
- NucleoSpin® Plant II:タカラバイオ
磁気ビーズ法
関連する記事はこちら
参考文献
- Jina, H., Rajkumar, K., Pranab, B.(2020). The Chemistry Behind Plant DNA Isolation Protocols, Biochemical Analysis Tools – Methods for Bio-Molecules Studies, Oana-Maria Boldura, Cornel Baltă and Nasser Sayed Awwad, IntechOpen.
- Lu, Y. (2011). Extract Genomic DNA from Arabidopsis Leaves (Can be Used for Other Tissues as Well). Bio-101: e90. DOI: 10.21769/BioProtoc.90.
- Fabian, F.(2016). Extraction of genomic DNA using “Edwards” buffer V.1. Protocols.io. DOI: dx.doi.org/10.17504/protocols.io.grdbv26.
- K. Edwards, C. Johnstone, C. Thompson.(1991). A simple and rapid method for the preparation of plant genomic DNA for PCR analysis. Nucleic Acids Research, Volume 19, Issue 6, 1349.










コメントを残す